imsel olarak en eski proteinlerdendir (Bölüm
189'a bakiniz). Klasik yol erken dönem komp-
leman eksiklii olan hastalar, opsonik aktivite
kaybindan dolayi sadece tekrarlayan enfeksi-
yonlara maruz kalmayip lupus geliimine de
oldukça eilimlidirler. Komplemanin gösteril-
mi en önemli rolü apopitoza giden hücrelerin
ortadan kaldirilmasi ve toleransin oluturul-
masidir.
organ hasarina doal immün sistemin katkisi,
enflamasyonlu dokuda makrofaj ve nötrofille-
rin gösterilmesi eklindedir. Otoimmün has-
taliklardaki patolojik yanitta bu hücreler sik
görülmemekle birlikte otoenflamatuar hasta-
liklarda sorunun kaynai nötrofillerdir. Bunla-
rin patofizyolojisi bölüm 209'da ayrintili olarak
tartiilmitir ama burada ana hatlariyla açikla-
mak yararli olacaktir.
ate sendromu, mevalonat kinaz eksiklii ve
CIAS1 otoenflamatuar bozukluklar, nispeten
daha az anlailmi çok genli bozukluklarin ay-
dinlatilmasina yardimci olmaktadir. Tüm tek
gen bozukluklarinda enflamatuar yolda IL-1
ve IL-18 ekspresyonunda problem vardir (
vasyon sonrasi düzenin tekrar kurulmasindan
sorumludur. Nötrofillerin yaam beklentisi
sadece 18-24 saattir. Uygunsuz enflamasyon
devamliliini önlemek için bakteri fagositozu
sonrasi nötrofillerin apopitozu artar. Bilinen
çou otoenflamatuar hastalikta nötrofil hüc-
re ölümü gecikir, enflamasyon uzar. NALP3/
CIAS1 ilikili sendromlarda cryopyrin defekti
artan hücre ölümlerine yol açar. Halbuki bu,
apopitozda görüldüü gibi immünolojik olma-
yip oluan bu farkli ölüm tipi daha fazla enfla-
masyona yol açmaktadir.
kontrol mekanizmasi arasinda kritik bir denge
olduu açikça görülmektedir. Hücrelerin ve si-
tokin ürünlerinin düzenlenmesinde bozulma
son derece kritik olmakta ve bu yol ile hasara
neden olabilmektedir.
id organlarda olgunlamakta, plazma hücresi
haline geldikten sonra dolaimdan kemik ilii-
ne geri dönmektedir. Geliimin hemen hemen
her basamainda denetleme olmakta, otore-
aktif B hücrelerinin sürekliliine ve hasara yol
B hücresinin evrimi sirasinda otoreaktif du-
rum geliimini önlemede kritik olmakta fakat
rekombinasyon olaylari immünglobulin mole-
kül ürünlerini rastgele seçerek otoreaktif duru-
ma yol açabilmektedir. Bu stratejilere ramen
periferde belli bir miktarda otoreaktif hücre
bulunmaktadir. Bu hücreler T hücreye yardim
için yarimakta, kisaca T hücrenin hayatta ka-
limini sadece B hücre salamamaktadir. Genel
olarak B hücresi için ayni türden yardim gerek-
mekte (T hücre ve B hücre benzer antijenleri
tanir), fakat bu gereksinim T hücresi için mev-
cut deildir. T hücrelerinin, enfeksiyon sirasin-
da spesifik olmayarak otoreaktif B hücrelerine
yardim ettii düünülmektedir. Benzer ekilde
fare modellerinde olduu gibi B hücre, nere-
deyse her zaman otoimmünite geliimi için
delesyon yeteneini deitirmitir.
hücre öncülleri timusa girer ve ya veya
T hücre reseptörü tair duruma gelirler. T
hücre geliimine kiyasla T hücre geliimi
hakkinda daha az bilgi mevcuttur. T hüc-
releri timus içinde kemokin uyarisina yanit
olarak gelimektedir. Bunlar ikili negatif T
hücreler olarak kapsül altinda çoalir, çünkü
bu hücrelerde CD4 ve CD8 yoktur. Bu noktada
T hücreleri, T hücre reseptör genlerini yeniden
düzenleme yoluna gider. T hücreleri ile stromal
komedüller yapinin geliimi için gerekmekte-
dir, bu da uyarinin timus epiteli boyunca dola-
tiini düündürmektedir. Baarili bir yeniden
düzenleme ile T hücreleri CD4 ve CD8'in iki-
sini de eksprese etmeye balarlar ve ikili pozitif
(DP) T hücreleri olarak adlandirilir. Bu hüc-
reler çok siki elemeye urarlar. Balangiçta ol-
dukça hareketli DP T hücreleri stromal hücre-
lerle etkileir. T hücre reseptörleri kendi MHC
ile karilikli etkileerek uyariyi alir, oysa tanima
yeteneine sahip olmayan T hücrelerde ölüm
oluur. Yaayan DP T hücrelerde ilk tarama
medullaya göç ederken olur, çeitli doku spesi-
fik antijenlere kari reseptör testi yapilir. Bu en
az bir transkripsiyon faktörü tarafindan uyaril-
mi gen düzenlenmesinde arti olarak tanim-
lanmitir, aksi takdirde timus içinde ifade edil-
mez. Timus "kendi için ayna" durumuna gelir
ve böylece kendi reaktif T hücrelerinin negatif
elemesi oluur. Medulla içerisinde düzenleyici
T hücreleri de geliir. Medulla içerisinde daha
fazla gelime, ya CD4 ya da CD8 ifade edilme-
sine yol açar ve bu yolla tekli pozitif T hücre
oluur. Tekli pozitif T hücreleri, timusdan çikip
perifere giderler. T hücre sadece MHC ile anti-
jeni tanir. CD4 T hücre MHC Class II ile, CD8
T hücre MHC Clas I ile antijeni tanir. Dend-
ritik hücreler, makrofajlar ve B hücreleri esas
antijen sunan hücrelerdir. Bunlarin her biri, e
uyaran moleküllerin düzenlenmesini arttirir,
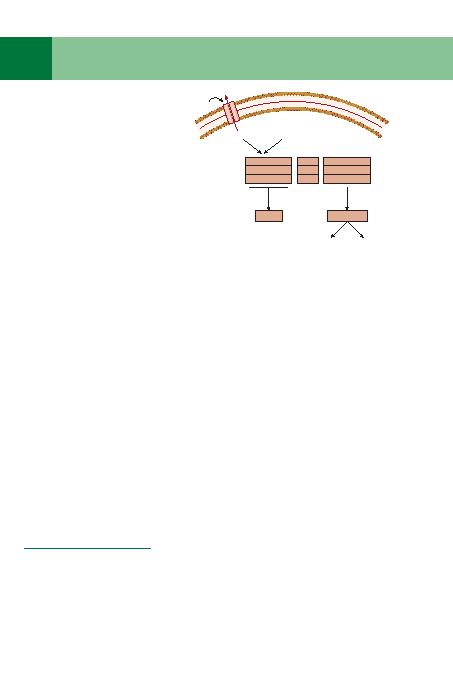
Asit
NALP 3
NALP 3
Prokaspaz 1
Prokaspaz 1
ASC
ASC
leri, bakteri hücre duvar¿ ürünleri ve baz¿ viruslerle uyar¿labilmektedir. Klasik inflamazom NALP3/CIAS1
(pirin 3 alan¿ içeren, NOD-benzeri reseptör ailesi), ASC (apopitoz iliùkili partikül benzeri protein içeren
bir CARD) ve prokaspaz'dan oluùur. Bu kompleksin aktivasyonu bölünmeye neden olur ve prokaspaz
1 ve aùaö¿ yönde IL-1
sendromu ve ailevi soöuk ürtiker ile iliùkilidir. Bu vakalardaki mutasyonlar kronik IL-1