esas yol; oksijenin, mitokondrideki elektron transfer (aktarma)
sistemi taraf>ndan redüksiyonu (indirgenmesi) reaksiyonunda
adenozin difosfat>n oksidatif fosforilasyonudur. jen yoklu¤unda ATP üretebilen, vücut s>v>lar>ndan veya gliko-
jenin hidrolizinden elde edilen glukozun kullan>ld>¤> glikolitik
yoldur. Dolay>s>yla, daha yüksek glikolitik kapasitesi olan (ka-
raci¤er gibi) dokular, oksidatif metabolizman>n zedelenme ile
inhibisyonu yüzünden ATP düzeyleri düflmeye bafllad>¤>nda
daha avantajl>d>rlar.
ATP'nin, normalin %5-%10'undan daha düflük düzeylere
inmesi çok say>da kritik hücresel sistemi yayg>n olarak etkiler:
Plazma membran>ndaki enerji ba¤>ml> sodyum pompas>-
n>n (ouabain-duyarl> Na+, K+-ATPaz) etkinli¤i azal>r. Bu ak-
tif tafl>ma sisteminin ATP konsantrasyonunun azalmas> ve
ATPaz etkinli¤inin artmas> nedeniyle çöküflü, sodyumun
hücre içinde birikmesine ve potasyumun hücre d>fl>na da¤>l-
mas>na neden olur. Erimifl haldeki maddelerin miktar>ndaki
net art>fl>n> izoosmotik olarak su giriflinin izlemesiyle, hücre
flifler ve endoplazmik retikulum genifller (bak>n>z fiekil 1-8).
Oksijen veya glukozdan yoksun kalan hücrelerde prote-
inler yanl>fl katlanabilir ve böyle katlanan proteinler, kat-
lanmam>fl protein yan>t> olarak adland>r>lan bir hücresel
reaksiyonu tetikleyerek hücre zedelenmesine, hatta ölümü-
ne neden olabilirler. Bu süreç, bölümün sonraki k>s>mlar>n-
da anlat>lmaktad>r. Proteinlerin hatal> katlanmas>; hücre, s>-
cakl>k gibi streslerle karfl>laflt>¤>nda ve proteinler enzim
(afla¤>da anlat>lan Ca2+'a yan>t veren enzimler gibi) veya
serbest radikaller taraf>ndan parçaland>¤>nda da görülür.
Ca
2+
pompas>n>n yetersizli¤i hücre içine afla¤>da belirti-
len çok say>da hücresel komponent üzerinde hasarlay>c>
etki yapan Ca
2+
girifline yol açar.
Uzam>fl veya kötüye giden ATP azalmas>, ribozomlar>n
kaba endoplazmik retikulumdan ayr>lmas> ve polizomlar>n
monozomlara ayr>flmas> ile kendini gösteren protein sen-
tez aparat>nda bozulmaya ve bunu takiben protein sente-
zinde azalmaya yol açar. Sonunda mitokondrial ve lizo-
zomal membranlarda geri dönüflsüz hasar oluflur ve hücre
nekroza u¤rar (bak>n>z fiekil 1-8).
Hücrelerdeki oksijen veya glukoz yoksunlu¤u proteinle-
rin kötü katlanmas>na yol açabilir ve kötü katlanm>fl prote-
inler katlanmam>fl protein yan>t> olarak adland>r>lan hüc-
re zedelenmesine ve hatta ölümüne neden olan hücresel
reaksiyonu tetikler. Bu süreç bu bölümde daha sonra anla-
t>lacakt>r. Protein kötü katlanmas> ayr>ca strese maruz ka-
lan hücrelerde proteinler, s>cakl>k ve enzimler (afla¤>da
belirtilen Ca
2+
-duyarl> enzimler gibi) ve serbest radikaller
ile hasara u¤rat>ld>¤>nda da görülür.
Mitokondriler, hipoksi ve toksinler dahil hemen her tür
zedeleyici uyaran için önemli hedeflerdir. Hücre zedelenmesi-
ne, mitokondrilerdeki morfolojik de¤ifliklikler s>k olarak efllik
eder. Mitokondriler; oksidatif stres sonucu sitozolik Ca2+ art>-
fl>, fosfolipidlerin fosfolipaz A2 ve sfingomiyelin yollar>nda par-
çalanmalar> ve buradan kaynaklanan serbest ya¤ asitleri ve se-
ramid gibi lipid parçalanma ürünleri taraf>ndan zedelenebilir-
ler. Mitokondri zedelenmesi ço¤u kez, mitokondri iç membra-
n>nda mitokondrial geçirgenlik geçifli (MPT) denilen yüksek
iletimli bir kanal oluflmas>na neden olur (fiekil 1-12).
17
Seçici
olmayan bu aç>kl>k bafllang>ç evrelerinde geri dönüfllü olsa da,
süreci bafllatan uyar> kesilmedi¤inde kal>c> duruma gelerek mi-
tokondrial proton itici gücünün veya potansiyelinin sürdürül-
mesine engel olur. Membran potansiyelinin korunmas> mito-
kondrial oksidatif fosforilasyon için kritik oldu¤undan; geri dö-
nüflsüz mitokondrial geçirgenlik geçifli, hücre için bir ölüm
ferman>d>r. Mitokondri zedelenmesine, sitokrom c'nin sitoso-
le s>zmas> da efllik edebilir. Sitokrom c elektron tafl>ma zinciri-
nin ayr>lmaz bir parças> oldu¤u ve sitosolde apoptotik ölüm
yolaklar>n> tetikleyebildi¤i için (sonraki k>sma bak>n>z), bu pa-
tolojik olay da muhtemelen hücre ölümünün anahtar belirleyi-
cilerindendir.
HÜCRE <ÇKALS
Kalsiyum iyonlar> hücre zedelenmesinin önemli mediyatör-
leridir.
18
Sitosolik serbest kalsiyum, 1.3 mmol olan hücre d>fl>
düzeye göre son derece düflük konsantrasyonda (<0.1 mmol)
tutulur. Hücre içi kalsiyumun ço¤u mitokondrilerde ve endop-
lazmik retikulumda saklan>r. Bu tür gradyanlar membran yerle-
flimli, enerji ba¤>ml> Ca
2+
Mg
2+
- ATPazlar taraf>ndan modüle edi-
lirler. toksinler; hem Ca
2+
'un plazma membra-
n>ndan net içe ak>m> hem mitokondriler ve endoplazmik reti-
kulumdan Ca
2+
sal>nmas> nedeniyle bafllang>çta sitozolik kalsi-
yum konsantrasyonunda art>fla neden olurlar (fiekil 1-13). Daha
sonralar>, hücre içi kalsiyum düzeyinde süregiden yüksekli¤in
nedeni, membran geçirgenli¤indeki spesifik olmayan art>fllar-
d>r. Yükselen Ca
2+
'da potansiyel y>k>c> hücresel etkileri olan
birtak>m enzimleri aktiflefltirir. Kalsiyum taraf>ndan aktive edi-
len bu enzimler içinde ATPaz'lar (böylece ATP azalmas> h>zla-
n>r), fosfolipazlar (membran hasar>na neden olurlar), proteaz-
15
BÖLÜM 1
Hücresel Adaptasyonlar, Hücre Zedelenmesi ve Hücre Ölümü
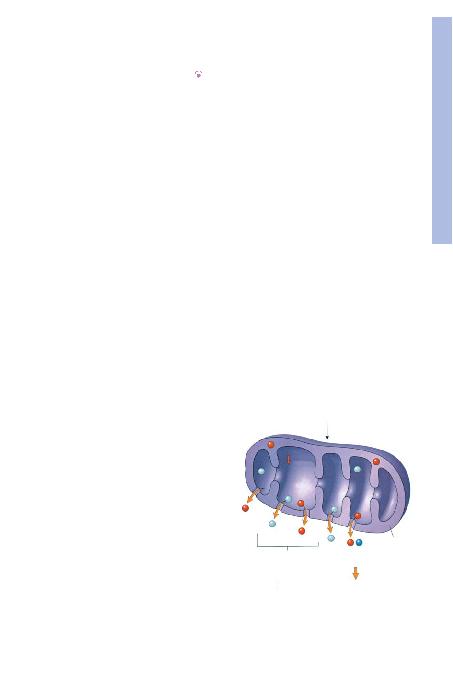
fiEKHücre zedelenmesinde mitokondrial fonksiyon bozuklu-
¤u.
Mitokondrial zedelenme veya disfonksiyon
(Sitoplazmik Ca
2+
art>fl>, oksidatif stres,
lipid peroksidasyonu)
Sitokrom c
H
+
Sitokrom c, di¤er
pro-apoptotik
proteinler
Mitokondrial
membran
Mitokondrial geçirgenlik
geçifli (kanal>, e.n.) (MPT)
Apoptoz
ATP üretimi
