également provenir des cellules endothéliales circulantes et des
cellules endothéliales progénitrices (24).
L'équipe de Vacca et al. a réalisé différentes études fonction-
nelles et génomiques (puce à ADN) comparant les cellules
endothéliales provenant de patients atteints de MM avec celles
provenant de patient atteints de GMSI, ainsi qu'avec des cel-
lules endothéliales provenant de cordons ombilicaux (HU-
VECs) (25). Ces études indiquent que les cellules endothéliales
isolées des patients souffrant de MM diffèrent des HUVECs en
ce qui concerne leur croissance, leur profil génétique et la sé-
crétion des facteurs de croissance. Les auteurs ont ainsi déduit
que les cellules endothéliales avaient un phénotype tumoral
caractérisé par des taux élevés de prolifération, de survie et
d'expression de plusieurs marqueurs vasculaires (tels que Tie-2,
VEGFR-2, FGFR-2, CD105-endoglin ou encore la VE-cadherin).
férencier en cellules endothéliales. Elles sont multipotentes et
possèdent certaines caractéristiques des cellules souches telles
été isolées par l'équipe de Asahara et al. à partir de sang hu-
main avec l'aide du marqueur membranaire CD34, ainsi qu'avec
d'autres marqueurs endothéliaux (26). Ils ont observé que ces
cellules hématopoïétiques se différenciaient in vitro et sem-
blaient s'incorporer aux sites angiogéniques dans de multiples
modèles d'ischémie in vivo. Les cellules endothéliales progéni-
trices partagent avec les cellules endothéliales matures et les
cellules souches certains marqueurs qui rendent leur distinc-
tion difficile (27-29). Trois antigènes (AC133, CD146 et CD45)
semblent cependant être utilisés pour faire la différence entre
cellules hématopoïétiques et cellules endothéliales (30, 31).
liales progénitrices ont également été étudiées par Zhang et al.
(32). Le nombre de cellules endothéliales circulantes est aug-
menté dans le sang des patients souffrant de MM et est cor-
rélé avec d'autres indicateurs de la maladie, comme par
exemple le niveau de protéine M et de microglobuline- 2. La
co-expression du récepteur du facteur de croissance endothé-
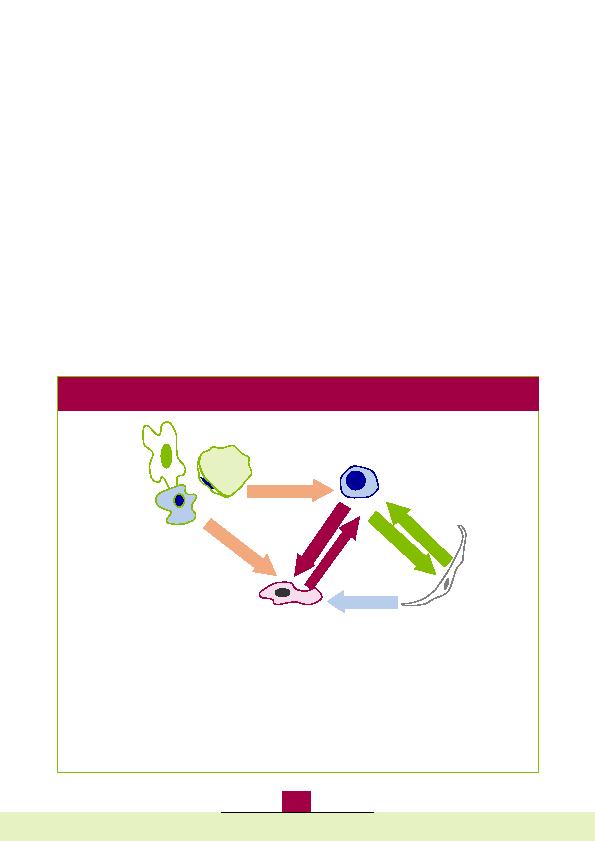
de cytokines intervenant dans le processus angiogénique par les fibroblastes (VEGF, FGF-2, IGF-1, OPN). Ces cytokines peuvent dès
lors stimuler la prolifération, la migration, la croissance et la survie des cellules endothéliales. Les cellules myélomateuses produisent
également elles-mêmes des cytokines affectant la prolifération et la migration des cellules endothéliales (VEGF-A, HGF, IGF-1, ANG-1,
OPN), ainsi que des protéinases (MMP2, MMP9, ADAM23, ADAMTS9) qui contribuent au processus angiogénique en dégradant la
matrice extracellulaire et les membranes basales. En retour, les cellules endothéliales peuvent supporter la croissance et le homing des
cellules cancéreuses en sécrétant différentes chémokines (IL-8, SDF-1, MCP-1), ainsi que des facteurs de croissance (VEGF, IGF-1, IL-6,
bFGF, HGF, OPN). Les adipocytes, présents dans la moelle osseuse et dont le nombre augmente avec l'âge, produisent également des
cytokines pro-angiogéniques (VEGF, FGF9), alors que les macrophages associés aux tumeurs permettent la transformation des cellules
endothéliales contribuant à la néo-vascularisation au sein de la tumeur.
cellules endothéliales supportent l'angiogenèse et le développement tumoral.