lié au mécanisme d'action, on n'a pas de réponse, même si on
suppose que l'inhibition du PlGF en est peut-être responsable.
Cela dit, dans l'étude TML, ce sont les patients qui toléraient
bien le bevacizumab qui ont continué; il est donc logique que
la tolérance générale ait été bonne. Il ne faut donc pas compa-
rer directement ces deux études, même si le taux de réponses
obtenu dans VELOUR est nettement plus élevé que celui que l'on
a observé dans TML. Mais il faut savoir que, dans la mesure où
VELOUR était prévue pour obtenir l'enregistrement de l'afliber-
cept, les patients enrôlés devaient prendre leur traitement à
la dose complète, ce qui n'a pas été le cas dans TML, où des
réductions de dose étaient permises, ce qui peut expliquer la
tolérance. Quoi qu'il en soit, il faut retenir de VELOUR l'activité
de l'aflibercept en deuxième ligne métastatique, qu'il y ait eu ou
non prétraitement par bevacizumab, l'allongement de la survie
globale, avec des chances de survie qui s'élèvent à 28% après
2 ans, et le taux de réponse élevé (19,8 vs 11,1%; p = 0,0001).
qu'il n'a pas été prévu de réaliser une analyse des biomarqueurs
afin de déterminer les meilleurs répondeurs. Mais cet aspect est
maintenant abordé dans un grand projet qui collecte les échan-
tillons tumoraux des patients traités dans l'étude VELOUR.
d'efficacité après progression sous
bevacizumab?
sieurs possibilités thérapeutiques qui nous permettent d'offrir des
deuxième et troisième lignes, et même au-delà, dans des condi-
tions de confort et de qualité de vie tout à fait acceptables. Il
ne faut pas oublier que les anti-EGFR peuvent également être
proposés après progression sous anti-angiogénique.
Par ailleurs, il existe plusieurs raisons pour lesquelles le schéma
FOLFIRI a été choisi dans VELOUR. Parmi celles-ci, il y a le
fait que les patients avaient reçu FOLFOX en première ligne,
mais aussi parce qu'il semble qu'il y ait une belle complémen-
des essais de phase I.
expérience, que proposeriez-vous comme
algorithme si l'aflibercept pouvait entrer
en compte?
tine, j'opterais volontiers en deuxième ligne, en cas de mutation
KRAS, pour l'une ou l'autre des solutions suivantes: FOLFIRI +
bevacizumab, FOLFIRI + aflibercept ou, en cas de contre-indi-
cations à un inhibiteur de l'angiogenèse, FOLFIRI seul. En cas
de progression rapide en première ligne, j'opterais plutôt pour
l'association avec l'aflibercept. Par contre, chez les patients qui
ont connu une bonne réponse, et de longue durée, à l'associa-
tion avec le bevacizumab, je continuerais ce dernier, car il est
en outre bien toléré. J'agirais de la même manière en cas de
KRAS wt. Dans cet algorithme, je proposerais donc surtout un
anti-EGFR en troisième ligne pour les patients KRAS wt, avant
de passer en quatrième ligne au regorafenib. La survie moyenne
est de l'ordre de 2 ans à 2 ans et demi à la condition d'être en
bon état général et que le patient ait été mis au courant de
l'objectif du traitement, qui est le contrôle de la maladie. On
peut bien sûr aussi commencer avec un anti-EGFR chez cer-
tains patients en première ligne, surtout si l'on veut transfor-
mer des métastases potentiellement résécables en métastases
réellement résécables.
sation en une ou deux phrases?
acceptable et que l'on peut gérer sans grosses difficultés, que l'on
peut considérer comme une option intéressante à partir de la
seconde ligne de traitement du cancer colorectal métastasé. Il a
certainement un rôle à jouer chez les patients atteints d'un car-
cinome du côlon métastasé en progression après oxiplatine. Un
inhibiteur de l'angiogenèse peut donc également avoir un effet en
deuxième ligne.
nique un peu différent du bevacizumab.
En quoi est-ce important?
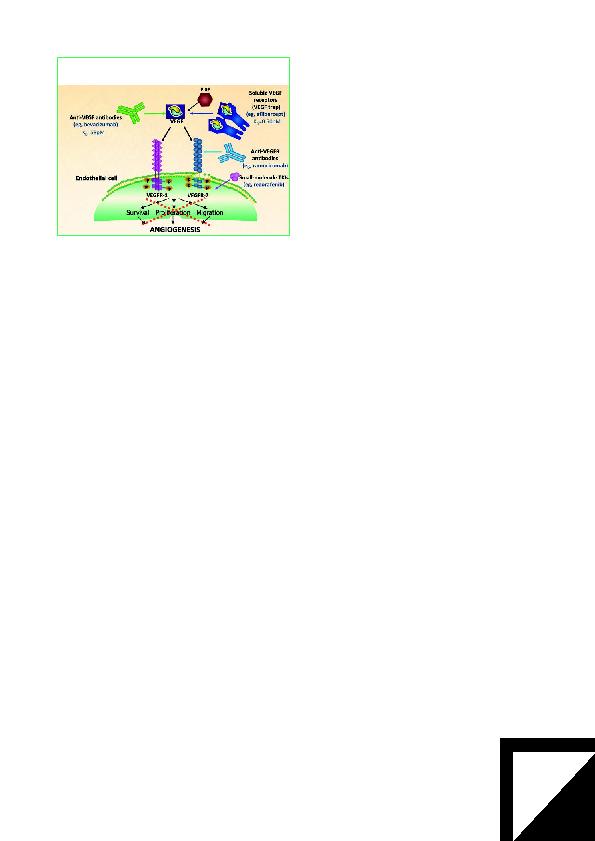
teur de l'angiogenèse doté d'un mécanisme d'action unique. Il
s'agit en effet d'une protéine de fusion soluble composée de
fragments du domaine extracellulaire des récepteurs de type 1
et 2 du VEGF (VEGF-R1 et VEGF-R2) associés à un fragment
Fc d'IgG1 humaine. Ce composé permet de «piéger», avec une
affinité cent fois supérieure à celle du bevacizumab, les dif-
férentes isoformes du facteur de croissance de l'endothélium
vasculaire A (VEGF-A), mais aussi le VEGF-B et le facteur de
croissance placentaire (PIGF), soit d'autres facteurs de crois-
sance angiogénique qui semblent jouer un rôle dans l'angioge-
nèse et la croissance tumorales (Figure 1). L'aflibercept se lie
par ailleurs au VEGF-A, au VEGF-B et au PIGF avec une plus
grande affinité que leurs récepteurs naturels. Cependant, si les
études précliniques ont montré que le VEGF-B et le PlGF ont
un rôle dans l'angiogenèse, on ne sait pas encore si le blocage
de tous ces facteurs ensemble entraîne des effets additionnels
au simple blocage du VEGF-A. Cela dit, le concept étant inté-
ressant (car susceptible de prévenir ou d'aller au-delà de cer-
taines résistances, puisqu'il peut bloquer des voies alternatives
de l'angiogenèse) et les études préliminaires concluantes (une
étude de phase I a suggéré une bonne efficacité antitumorale de
l'association aflibercept/5FU-irinotecan), il devenait logique de
l'évaluer dans le contexte de la 2
5-fluoro-uracile, leucovorin, irinotecan) à ce même traitement
de 2
tine, éventuellement en association avec le bevacizumab. Cette
étude est positive pour son objectif principal, la survie globale, qui
atteint 13,5 mois (vs 12,06 mois; HR = 0,817; p = 0,0032). Elle
est positive également pour la survie sans progression (6,9 mois
vs 4,67 mois; HR = 0,758; p = 0,00007) et le taux de réponse
objective (19,8% vs 11,1%; p = 0,0001). Ce taux élevé de
réponse, un taux jamais observé sous bevacizumab, est une des
forces de VELOUR. Mais cette étude est également particulière
dans la mesure où elle avait prévu l'analyse des données du sous-
groupe de patients qui avaient reçu du bevacizumab en première
ligne (environ 30%). On sait depuis peu en effet que la prolonga-
tion du bevacizumab après progression améliore la survie (3), ce
qui a été également le cas lorsqu'on change d'anti-angiogénique
en passant du bevacizumab à l'aflibercept. En pratique, l'analyse
par sous-groupe a montré que le bénéfice de l'aflibercept était
observé chez les patients n'ayant pas reçu de bevacizumab anté-
rieurement (n = 853; HR = 0,79) et qu'il existait également
une tendance, mais non significative (en raison d'un nombre rela-
tivement restreint de patients), chez les patients ayant progressé
sous un premier traitement contenant du bevacizumab (n =
373; HR = 0,86). On entre ainsi dans un concept qui va un peu
au-delà de ce que l'essai TML avait mis en évidence (3).
comparables...
ratif direct, on peut constater que les résultats sont comparables
avec un peu plus de toxicité dans les essais avec l'aflibercept:
diarrhée, stomatite, neutropénie, neutropénie fébrile, fatigue et
asthénie se rencontrent plus fréquemment dans le groupe FOL-
taux métastatiques est de savoir s'il est bénéfique d'administrer en deuxième ligne un traitement anti-
angiogénique après progression. C'est dire l'intérêt de l'essai VELOUR (1), première étude à montrer
l'efficacité d'un traitement anti-angiogénique autre que le bevacizumab dans le traitement des cancers
colorectaux métastatiques, en combinaison avec la chimiothérapie. Cette étude a démontré un effet
favorable de l'aflibercept en combinaison avec FOLFIRI en deuxième ligne. Poursuivre un traitement
anti-angiogénique (ou en tout cas introduire l'aflibercept) dans un sous-groupe de patients ayant reçu
du bevacizumab en première ligne a donc du sens. Le point avec le Pr Eric Van Cutsem (KU Leuven).