exposée de façon intermittente et non chronique au soleil. La
mutation la plus fréquente (90%) conduit à la substitution d'un
acide aminé en position 600 de la protéine BRAF (V600E) (7).
Cependant, des mutations sont aussi observées dans les naevi
sans transformation maligne; d'autres altérations géniques
semblent dès lors nécessaires pour le développement d'un
mélanome (6, 7). La détection de cette mutation permet de
proposer au patient une thérapie ciblée par inhibiteurs sélectifs
de la protéine mutée.
Les mutations de NRAS sont moins fréquentes (25%) et
rarement associées à celles de BRAF.
Les mutations de BRAF et NRAS sont rares dans les mélanomes
se développant en peau chroniquement photo-exposée, ainsi
que dans les mélanomes muqueux et des zones acrales (6, 7).
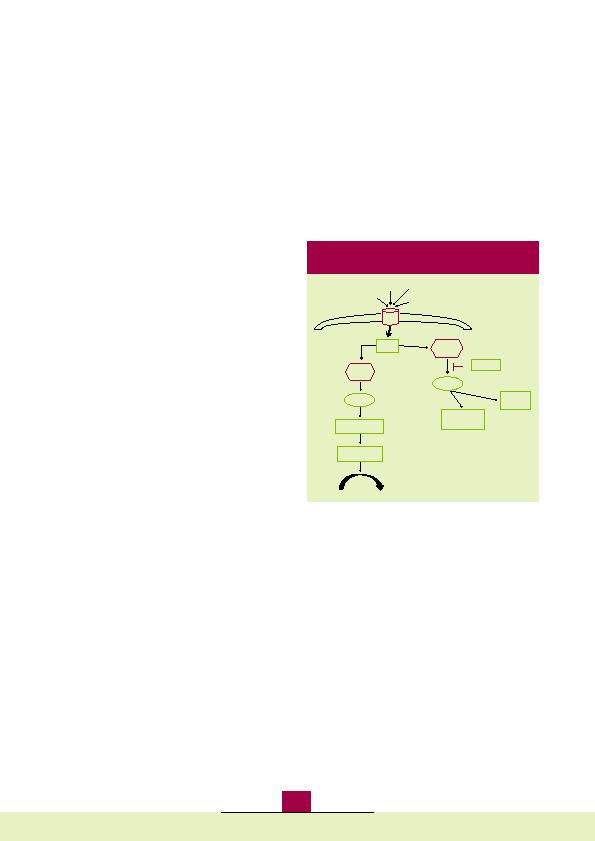
3-kinase (PI3K) / AKT / phosphatase and tensin homolog (PTEN)
/ mammalian target of rapamycin (mTOR) impliquant le gène
suppresseur de tumeur, pro-apototique, PTEN. L'activation de
PI13K, par des facteurs de croissance via RAS, induit des phos-
phorylations en cascade, dont celle de AKT, qui promeut la sur-
vie cellulaire via l'activation de facteurs anti-apoptotiques tels
que BCL2 et via l'inhibition de complexes suppresseurs de tu-
meurs (TSC1/TSC2) (15). D'autre part, l'inactivation de TSC1/
TCS2 stimule l'activité de mTOR, favorisant la capture d'élé-
ments nutritifs nécessaires à la croissance cellulaire (13). Cette
voie inhibe donc l'apoptose. La protéine PTEN dégrade les pro-
duits de PI3K, inhibant ainsi cette voie de prolifération (13).
PTEN est exprimé dans presque tous les naevi bénins et dyspla-
siques (2), tandis qu'une réduction fonctionnelle est observée
dans 20% des mélanomes primaires (13). Cette diminution
d'activité n'est que partiellement liée à des mutations inhibitrices
de PTEN (2, 13, 14). La perte fonctionnelle de PTEN est positi-
vement corrélée avec l'indice de Breslow (13).
croissance
entre des récepteurs membranaires et leurs ligands. Ainsi, l'acti-
vation peut être la conséquence d'une hyperstimulation de ces
récepteurs (IGF1R, MET, FGF, R-SCF/c-KIT) sans anomalie des
facteurs en aval de la voie (6).
Des mutations activatrices de c-KIT sont rapportées dans 39%
des mélanomes muqueux, dans 36% des mélanomes des zones
acrales, dans 26% des mélanomes en peau photo-exposée
chronique et dans 80% des mélanomes oculaires (2, 6).
code pour un récepteur membranaire exprimé par les mélano-
cytes épidermiques et dont le ligand est -MSH. L'activation de
MC1R aboutit à l'activation du facteur de transcription MITF et
d'enzymes impliquées dans la synthèse de l'eumélanine (2).
De nombreux variants de MC1R sont décrits: trois d'entre
eux sont associés à une réduction de leur activité, détermi-
nant un phénotype Red Hair Color, tandis que d'autres sont
associés à une sensibilité marquée au soleil en l'absence de ce
phénotype. Ces variants représentent un facteur de risque de
développer un mélanome (2, 7).
thérapies antitumorales. La résistance du mélanome à ces trai-
tements peut être due à des mécanismes permettant aux
mélanocytes tumoraux d'échapper à l'apoptose (6).
Deux voies principales convergent pour induire l'apoptose:
- la voie intrinsèque ou mitochondriale met en jeu les gènes
P3L) sont proapoptotiques et d'autres anti-apoptotiques
(BCL2, MCL1, BCL-XL). Elle aboutit à la perméabilisation
de la membrane mitochondriale avec libération de facteurs
apoptotiques dans le cytosol et activation de la cascade des
caspases et fragmentation de l'ADN (6);
son ligand (Fas ligand, TRAIL). La cascade des caspases est
ainsi déclenchée (6).
le mélanome.