comparer le médicament et le placebo, et études cliniques présentant des
marges d'innocuité importantes, ce qui entraîne le refus d'inclure une pro-
portion élevée de patients dans l'étude. Certains risques d'innocuité sont
en conséquence potentiellement sous-estimés, les médicaments de l'étude
étant finalement prescrits à une population étendue de patients.
veloppement d'autres affections par des patients psoriasiques ne peut être
comparé à celui de la population saine. Les patients psoriasiques présentent
notamment un risque accru de lymphome et d'autres malignités, même sans
traitement par inhibiteurs du TNF (13). Un traitement par inhibiteurs du TNF
pourrait toutefois impliquer un risque plus élevé de cancer de la peau, même
en l'absence d'une thérapie lumineuse préalable (14).
est indissolublement lié à la maladie contre laquelle ils ont été prescrits.
Si de nombreux biomédicaments peuvent effectivement être administrés
contre différentes pathologies, le profil d'innocuité à long terme associé à
une affection donnée ne sera pas nécessairement analogue pour une autre
maladie. Une étude sur l'adalimumab a fait état d'écarts importants liés aux
différentes utilisations en ce qui concerne le développement d'infections
graves et d'un risque largement inférieur en cas d'administration contre le
psoriasis et la spondylarthrite ankylosante (15). Il apparaît donc essentiel de
disposer d'un profil d'innocuité correspondant au patient psoriasique pour
chaque biomédicament.
bonne méthode pour obtenir des données d'innocuité correctes à long terme.
L'objectif est de continuer après une étude clinique à suivre des patients
pendant une période complémentaire d'une à cinq années sur la base de la
même thérapie, comme si ces sujets étaient toujours inclus dans l'étude en
question. Ce type de recherche a été mené pendant cinq ans avec l'ustekinu-
mab afin de suivre l'innocuité du médicament à long terme et a indiqué qu'il
n'existait pratiquement aucune différence entre le court et le long terme quant
au risque de développement d'infections graves ou de cancers de la peau
autres que le mélanome, ce qui semble plutôt rassurant (16).
convient de prêter plus particulièrement attention au développement d'évé-
nements cardiovasculaires majeurs (MAjor Cardiovascular Events, MACE)
chez les patients prenant des médicaments biologiques, soit, entre autres,
l'infarctus aigu du myocarde et l'AVC ainsi que le décès consécutif à ces
événements. Etant donné le risque cardiovasculaire accru, les événements
MACE entraîneront toujours, quelle que soit la thérapie administrée, le décès
de certains patients psoriasiques. L'étude OLE sur l'ustekinumab a mis en
évidence un risque MACE comparable, pour une utilisation de trois à quatre
ans, par rapport à une population analogue n'ayant pas été traitée par uste-
kinumab, ce qui laisse présumer un bon profil de risque cardiovasculaire sûr
à long terme (16).
traitements antipsoriasiques oraux et à la thérapie lumineuse ont mis en
lumière une tendance à une proportion inférieure d'événements MACE en cas
de thérapie biologique. Aucune différence significative n'a été constatée entre
les différents biomédicaments (17-19). Il y a cependant lieu de noter que la
plupart des événements MACE surviennent chez des patients souffrant de
troubles cardiovasculaires non contrôlés et qu'aucun des médicaments bio-
logiques disponibles ne peut pour l'instant être considéré comme cardiopro-
tecteur. Il reste primordial de veiller à une gestion adéquate des risques car-
diovasculaires chez les patients psoriasiques, de déterminer régulièrement la
pression artérielle et le taux de cholestérol et, le cas échéant, de procéder aux
corrections requises via une médication spécifique.
lorsqu'une thérapie n'est pas suffisamment efficace. Les médicaments bio-
logiques restent cependant des traitements de deuxième ligne, à administrer
après l'échec d'une thérapie lumineuse, de la ciclosporine et/ou du métho-
trexate. Les différences en termes d'induction-efficacité et le maintien de
l'efficacité constituent des critères décisifs pour le choix d'un biomédicament.
Les biomédicaments se caractérisent par un profil d'innocuité adéquat, sans
différence significative entre les divers inhibiteurs du TNF et l'ustekinumab.
Etant donné la proportion accrue de facteurs de risque cardiovasculaire chez
les patients psoriasiques, le contrôle et la correction de ces facteurs (hyper-
tension, cholestérol, etc.) ont une importance cruciale.
1.
2010;44(1):119-26.
population-based study. Arch Dermatol 2007;143(12):1493-9.
2006;296(14):1735-41.
calcification. Br J Dermatol 2007;156(2):271-6.
events. Am J Med 2011;124(8):775.e1-6.
psoriasis: a multicenter cross-sectional study in Germany. Dermatology 2008;216(4):366-72.
PsoHealth 2007. J Dtsch Dermatol Ges 2008;6(8):640-5.
European consensus. Arch Dermatol Res 2011;303(1):1-10.
network meta-analysis of randomized controlled trials. Br J Dermatol 2012;166(1):179-88.
Dermatology 2010;221(Suppl 1):43-7.
controlled trial (PHOENIX 1). Lancet 2008;371(9625):1665-74.
2006. EULAR 2009. Abstract FRI0201.
2012;11(3):300-12.
Dermatology and Venereology, 20-24 October 2011, Lissabon.
& Venereology (EADV) congress, Prague 2730 September 2012. Oral session FC02.7.
Annual Meeting; February 48, 2011; New Orleans.
raison de son efficacité élevée démontrée, joue un rôle important pour les
patients chez qui d'autres thérapies se sont révélées insatisfaisantes. L'effi-
cacité constitue un critère déterminant pour le choix des biomédicaments ad
hoc. Les différences en termes d'induction-efficacité et le temps de réaction
ractérisent notamment par une phase d'induction rapide (jusqu'à la semaine
16), par comparaison au temps d'induction plus long du méthotrexate, des
fumarates et de l'étanercept (jusqu'à la semaine 24) (8). Selon une méta-
analyse de l'année 2011 portant sur l'induction-efficacité déterminée sur la
base d'études à court terme, les médicaments les plus efficaces sont l'inflixi-
mab et l'ustekinumab 90mg et 45mg, suivis par l'adalimumab et, finalement,
l'étanercept (
la chronicité du psoriasis chez la très grande majorité des patients concernés.
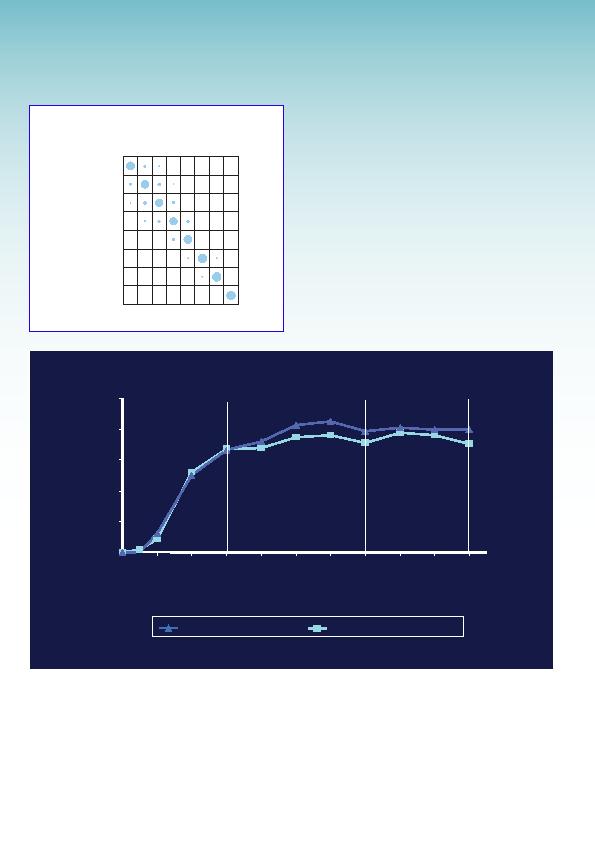
Une étude portant sur l'ustekinumab a mis en évidence une amélioration du
PASI rapide au cours des douze premières semaines et une amélioration du
PASI 75 à 28 semaines (11) (
ment sur l'efficacité à atteindre et à maintenir, l'innocuité des médicaments
joue par ailleurs un rôle tout aussi important. Or il est parfois difficile de
comparer les différents médicaments disponibles: études cliniques intégrant
uniquement un bras placebo au cours des douze premières semaines, ce
pour le traitement du psoriasis.
patient